

 In questa pubblicazione viene illustrato un risultato tuttora in fase sperimentale ma che potrebbe rivelarsi una svolta nel trattamento della Sindrome Respiratoria Acuta Grave in corso di COVID-19. La Malattia da Coronavirus 2019, definita come COVID-19, è una nuova malattia causata da un virus con un singolo filamento di RNA, chiamato Coronavirus (CoV) della Sindrome Respiratoria Acuta Grave (SARS) o SARS-CoV-2. L'espressione clinica della malattia varia da una affezione respiratoria lieve a una molto grave, quest’ultima colpisce circa un terzo dei pazienti e progredisce spesso in una grave insufficienza respiratoria o Sindrome da Distress Respiratorio Acuto (ARDS), con un'alta mortalità. I pazienti affetti da COVID-19 possono inoltre presentare un decorso clinico bifasico, cioè, dopo aver avuto un miglioramento iniziale, possono presentare un netto peggioramento. Ciò fa pensare che a causare il peggioramento della malattia sia un'attivazione immunitaria ritardata ed esagerata, piuttosto che non l'azione diretta del virus. In sostanza la causa della ARDS nella COVID-19 sarebbe un’eccessiva produzione di citochine e di conseguenza una esagerata risposta infiammatoria a livello polmonare. Questa situazione è stata definita come “Tempesta Citochinica”.
In questa pubblicazione viene illustrato un risultato tuttora in fase sperimentale ma che potrebbe rivelarsi una svolta nel trattamento della Sindrome Respiratoria Acuta Grave in corso di COVID-19. La Malattia da Coronavirus 2019, definita come COVID-19, è una nuova malattia causata da un virus con un singolo filamento di RNA, chiamato Coronavirus (CoV) della Sindrome Respiratoria Acuta Grave (SARS) o SARS-CoV-2. L'espressione clinica della malattia varia da una affezione respiratoria lieve a una molto grave, quest’ultima colpisce circa un terzo dei pazienti e progredisce spesso in una grave insufficienza respiratoria o Sindrome da Distress Respiratorio Acuto (ARDS), con un'alta mortalità. I pazienti affetti da COVID-19 possono inoltre presentare un decorso clinico bifasico, cioè, dopo aver avuto un miglioramento iniziale, possono presentare un netto peggioramento. Ciò fa pensare che a causare il peggioramento della malattia sia un'attivazione immunitaria ritardata ed esagerata, piuttosto che non l'azione diretta del virus. In sostanza la causa della ARDS nella COVID-19 sarebbe un’eccessiva produzione di citochine e di conseguenza una esagerata risposta infiammatoria a livello polmonare. Questa situazione è stata definita come “Tempesta Citochinica”.
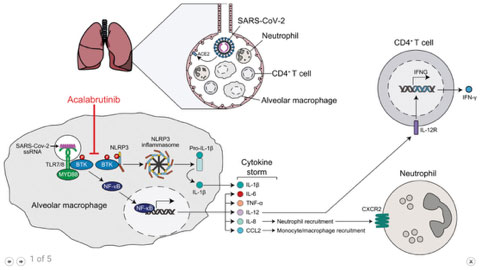
Fig. 1 Modello di iperinfiammazione dipendente da BTK in gravi COVID-19.
Il legame di SARS-CoV2 a ACE2 sull'epitelio respiratorio avvia l'infezione. I macrofagi inglobano le particelle virali contenenti RNA virale a singolo filamento (ssRNA). SsRNA può legarsi ai Toll Like Receptor TLR7 e TLR8. A valle dell'impegno dei TLR, si attiva il fattore nucleare kappa B (NF-κB) che dipende dall’intervento della Tirosino Chinasi di Bruton (BTK) con conseguente produzione di citochine e chemochine pro-infiammatorie. Si crea una 'tempesta di citochine' che può aumentare l’arrivo nel polmone di monociti / macrofagi e neutrofili durante la fase tardiva di gravi infezioni da COVID -19. Inibitori di BTK come acalabrutinib bloccano l'attivazione di NF-κB nei macrofagi, attenuando così la produzione di mediatori pro-infiammatori, come è stato dimostrato in un modello di danno polmonare indotto dall'influenza. Durante una grave COVID-19, i livelli elevati di interleuchina IL-1β in diversi pazienti COVID-19 indicano la attivazione della proteina NLRP3 con la formazione di un inflammasoma che converte pro-IL-1β in IL-1β matura. BTK si lega a NLRP3 e la fosforila, promuovendo così il suo assemblaggio in un inflammasoma. Inibitori di BTK come acalabrutinib inibiscono la produzione di IL-1β, mediata da inflammasoma, come osservato in un modello di danno polmonare indotto dall'influenza.
Conosciamo abbastanza bene come si sviluppa la risposta immunitaria infiammatoria nei confronti dei virus, perché studiata a fondo nell’influenza e questo modello sperimentale può essere applicato anche all’infezione del coronavirus SARS-CoV-2. Dopo il contagio da parte del virus, la prima risposta arriva dall’Immunità Innata, una difesa non specifica ma sempre pronta ad agire. I fanti di questa difesa sono i Macrofagi, che, come dice il nome, fagocitano (mangiano) il virus e le sue componenti presenti nell’ambiente: in particolare l’RNA virale. L’RNA virale all’interno dei macrofagi attiva due vie importanti dell’infiammazione: la prima si avvia tramite il legame dell’RNA virale con particolari recettori per i batteri e i virus, o Toll Like Receptors (TLR), questi a loro volta attivano un fattore nucleare KB (NFKB) che suscita una esagerata produzione di citochine pro-infiammatorie: IL-6, TNFα, IL-12, IL-8, CCL-2. La seconda via di attivazione dell’infiammazione, all’interno del Macrofago avviene tramite una proteina, chiamata NLRP che, avvertendo il pericolo dell’RNA virale crea una risposta infiammatoria, chiamata Inflammosoma che porta in definitiva alla produzione di grandi quantità di IL-1β. La straordinaria produzione di linfochine (Tempesta Citochinica) è responsabile dell’attivazione di molte cellule dell’infiammazione che convergono nei tessuti polmonari dove è presente il virus, condizionando l’aggravamento e l’instaurarsi di una ARDS.
Per controbattere questo fenomeno sono stati tentati dei trattamenti con anticorpi monoclonali anti Il-6, come molti sanno, della cui efficacia attendiamo ancora conferma. È chiaro però che controbattere l'anomala risposta immunitaria fin dalle prime fasi del processo di attivazione delle diverse citochine interessate dovrebbe dare un risultato migliore rispetto a contrastare l’azione di una sola linfochina. La Tirosina Chinasi di Bruton o BTK è una proteina che all'interno del Macrofago svolge un ruolo essenziale nell’attivazione iniziale di entrambe le vie dell’infiammazione (dei TLR e dell’inflammosoma) ed è quindi logico ipotizzare che la sua inibizione dovrebbe ridurre la produzione di tutte le linfochine in gioco con beneficio del paziente.
Prodotti a base di anticorpi monoclonali anti-Tirosino Chinasi di Bruton (BTK) esistono in commercio e sono approvati per il trattamento di alcuni tumori e fra questi si ricorda l'acalabrutinib (Calavi, Astra Zeneca). Un gruppo di ricercatori statunitesi del National Cancer Institute, in collaborazione con ricercatori del National Institute of Allergy and Infectious Diseases (NIAID), del Centro medico militare Walter Reed del Dipartimento della Difesa degli Stati Uniti e di altri quattro ospedali a livello nazionale, hanno condotto una sperimentazione di trattamento di alcuni pazienti di COVID-19 utilizzando acalabrutinib “off label”. Il farmaco biologico è stato usato in 19 pazienti con una diagnosi confermata di COVID-19, tutti ricoverati in ospedale, con bassi livelli di ossigeno nel sangue ed evidente infiammazione con impegno di citochine (Tempesta citochinica). Di questi pazienti, 11 ricevevano ossigeno supplementare e altri otto erano in ventilazione meccanica.
La maggioranza dei pazienti del sottogruppo con ossigeno supplementare, entro 1-3 giorni dall’inizio di acalabrutinib, ha manifestato un calo sostanziale dell'infiammazione con miglioramento della respirazione. Otto su undici di loro hanno smesso l'ossigeno supplementare e sono stati dimessi dall'ospedale. Nel sottogruppo di pazienti con ventilazione meccanica, solo quattro su otto, dopo trattamento con acalabrutinib sono stati in grado di uscire dalla ventilazione e due di loro sono stati dimessi. Quattro pazienti di questo gruppo non sono invece migliorati e due sono morti. Dopo il trattamento con acalabrutinib, i livelli di BTK e di interleuchina-6 (IL-6) sono diminuiti e sono aumentati i valori dei linfociti. I ricercatori hanno anche trovato valori aumentati di BTK e di IL-6 nei malati di COVID-19 rispetto a quelli trovati nei soggetti sani di controllo. Questi risultati suggeriscono che l’efficacia di acalabrutinib possa dipendere da un ruolo essenziale di BTK nel sostenere la “Tempesta Citochinica”. Va però ricordato che si tratta di risultati preliminari e che è importante aspettare i risultati di specifici studi controllati e randomizzati per una conferma basata su un’alta qualità dell'evidenza.
Fonte: Roschewski M. et al. Inhibition of Bruton tyrosine kinase in patients with severe COVID-19 Science Immunology, 05 Jun 2020